GUO Yuxiang, HUANG Liqiang, WANG Gang, WANG Hongzhi. Kompleksni elektrolit s dvostrukom litijevom soli: priprema i primjena u litij-metalnoj bateriji. Journal of Anorganic Materials, 2023, 38(7): 785-792 DOI:10.15541/jim20220761
Sažetak
Metalni Li je jedna od idealnih anoda za litij-ionsku bateriju visoke gustoće energije zbog svog visokog teorijskog specifičnog kapaciteta, niskog redukcijskog potencijala kao i obilnih rezervi. Međutim, primjena Li anoda pati od ozbiljne nekompatibilnosti s tradicionalnim organskim tekućim elektrolitom. Ovdje je polimerizacijom in situ konstruiran gel kompleksni elektrolit (GCE) sa zadovoljavajućom kompatibilnošću s metalnom Li anodom. Dvostruki sustav litijeve soli uveden u elektrolit može surađivati s polimernom komponentom, koja proširuje elektrokemijski prozor elektrolita na 5,26 V u usporedbi s 3,92 V komercijalnog elektrolita i postiže visoku ionsku vodljivost od 1×10-3 S· cm-1 također na 30 stupnjeva. Rezultati morfološke karakterizacije i elementarne analize površine Li anode pokazuju da GCE pokazuje očigledan zaštitni učinak na metalni litij u uvjetima dvostrukog sustava litijeve soli, a volumenski učinak i rast dendrita Li anode očito su inhibirani. U isto vrijeme, litij-metalna puna baterija, sastavljena s komercijalnim katodnim materijalom litij-željezo-fosfat (LiFePO4), pokazuje izvrsnu stabilnost ciklusa i performanse brzine. Stopa zadržavanja kapaciteta baterije doseže 92,95 posto nakon 200 ciklusa pri konstantnoj struji od 0,2C (1C=0.67 mA·cm-2) na 25 stupnjeva. Ova studija pokazuje da GCE može učinkovito poboljšati sigurnost, stabilnost i sveobuhvatnu elektrokemijsku izvedbu litij-metalne baterije, za koju se očekuje da će pružiti strategiju za univerzalni dizajn kvazi-krutog elektrolita.
Ključne riječi:metalik Li; in situ polimerizacija; gel složeni elektrolit
Otkako je 2020. postavljen cilj "dvostruki ugljik", Kina se suočava s reformom energetskog sustava bez presedana. Kina treba dovršiti duboko smanjenje emisija ugljika u sljedećih 30 godina, a zelena energija će postupno jačati dok ne zamijeni "monopolski" položaj tradicionalne fosilne energije. Kao važan dio sustava obnovljivih izvora energije, tehnologija litij-ionskih baterija privukla je široku pozornost nakon što se pojavila. Trenutačno, osim što su glavni energetski uređaj 3C elektroničkih proizvoda, primjena litijevih baterija u područjima automobilske industrije, zrakoplovstva i pametne mreže postupno raste, što postavlja veće zahtjeve za njihovu izvedbu. Kako bi se dobio duži domet krstarenja, litijeve baterije trebaju razviti sustav baterija s većom gustoćom energije. Među njima, očekuje se da će metalni litij s ultra-visokim specifičnim kapacitetom (3860 mAh g-1) i niskim redukcijskim potencijalom (-3.04 V (vs SHE)) postati anodni materijal za sljedeću generaciju baterija visoke gustoće energije. Međutim, kada je metalni litij u kontaktu s organskim tekućim elektrolitima, nuspojave se nastavljaju događati na sučelju, što dovodi do nekontroliranog rasta litijevih dendrita, probijanja unutarnjeg separatora baterije, uzrokujući kratke spojeve, pa čak i sigurnosne probleme. Kao odgovor na ovaj nedostatak, obično se razmatra korištenje čvrstog elektrolita umjesto tekućeg elektrolita kako bi se poboljšala sigurnost baterije. Međutim, njegova ionska vodljivost pri niskoj sobnoj temperaturi i loša međupovršinska kompatibilnost ozbiljno koče njegov daljnji razvoj i primjenu.
U tom kontekstu, elektroliti u gel stanju koji mogu uravnotežiti međupovršinske kontakte i ionsku vodljivost dobivaju sve veću pozornost. Tan Shuangjie i suradnici razvili su nezapaljivi elektrolit u obliku gela imobilizacijom organofosfata koji usporavaju plamen u polimernoj matrici polivinilen karbonata visoke mehaničke čvrstoće. Elektrolit ima prednosti visoke ionske vodljivosti i litij-ionskog prijenosnog broja, nezapaljivosti, visoke mehaničke čvrstoće i dobre elektrokemijske kompatibilnosti. Osim toga, gel elektrolit formiran unutar baterije polimerizacijom na licu mjesta ima karakteristike niske viskoznosti, jednostavnog rukovanja i snažne sposobnosti vlaženja, koji se može potpuno infiltrirati u aktivne materijale i proizvesti idealan međupovršinski kontakt, čime se postiže dobar put migracije iona . Na primjer, Guo Yuguoova istraživačka grupa pomiješala je tradicionalni monomer na bazi etera 1,3-dioksolan (1,3-dioksolan, DOL) s 1,2-dimetoksietanom (1,{{15} }Dimetoksietan, DME), komercijalni litij heksafluorofosfat (LiPF6) kao litijeva sol može istovremeno pokrenuti polimerizaciju otvaranja prstena DOL-a i novi elektrolit u stanju gela koji može raditi stabilno u litij-sumpornim baterijama i komercijalnim katodnim baterijama je dobiveno. Iako je polimer na bazi polietera jedan od najstabilnijih elektrolita za litijeve metalne anode, njegov uzak elektrokemijski prozor i niska ionska vodljivost na sobnoj temperaturi ograničavaju njegovu primjenu u baterijama visoke gustoće energije. Iako LiPF6 ima idealnu ionsku vodljivost i izvrsnu kompatibilnost s elektrodama, problem mu je slaba elektrokemijska stabilnost. Stoga, za razvoj elektrolita u gel-stanju s izvrsnim sveobuhvatnim performansama, potrebno je odabrati odgovarajuće polimerne domaćine, litijeve soli i druge komponente.
Kako bi se uravnotežio odnos između vodljivosti, stabilnosti visokog napona i kompatibilnosti elektroda, u ovoj studiji razvijen je kompozit kruto-tekuće GCE visokih performansi. Usvojena je metoda termički inicirane in situ polimerizacije, PEGDA je korišten kao monomer, dodano je miješano otapalo etilen karbonata i dietil karbonata, a LiTFSI i LiDFOB su uvedeni kao dvostruki sustav litijeve soli koji radi zajedno s polimernim komponentama. Uz poboljšanje elektrokemijske izvedbe, stabilnost sučelja između elektrolita i litijeve metalne anode dodatno je poboljšana.
1 Eksperimentalna metoda
1.1 Priprema GCE
LiTFSI, LiDFOB, EC i DEC (Suzhou Duoduo Chemical Technology Co., Ltd.) svi su bezvodni materijali za baterije. EC i DEC reagensi su pomiješani, a LiTFSI i LiDFOB su izvagani i otopljeni u otapalu. Pripremljeni elektrolit sustava dvostruke soli (tekući elektrolit, LE) bio je EC/DEC (volumenski omjer 1:1) otopina 1 mol/L LiTFSI i 0.2 mol/L LiDFOB. PEGDA (veća ili jednaka 99 posto, Mn=400) i azobisisobutironitril (Azodiizobutironitril, AIBN, 98 posto) kupljeni su od Shanghai Aladdin Reagent Co., Ltd. Otopina prekursora GCE pripremljena je miješanjem PEGDA i LE , a maseni udio PEGDA bio je 10 posto , 20 posto i 30 posto . Dodati 1 posto masenog udjela toplinskog inicijatora AIBN i dobro promiješati. Otopina prekursora PEGDA zagrijavana je na 70 stupnjeva 2 sata kako bi se dobili potpuno polimerizirani gel kompozitni elektroliti na bazi PEGDA, koji su nazvani GCE-x (x=10, 20, 30). Svi gornji pokusi provedeni su u bezvodnom pretincu za rukavice bez kisika.
1.2 Sastavljanje baterije
Baterijski sklop od CR2025 gumbaste ćelije (316 nehrđajući čelik, SS), litijskog metalnog lima (14 mm×0.45 mm, Li), aluminijske folije (razred baterije). Prema različitim zahtjevima ispitivanja, SS||SS baterije, Li||SS baterije, Li||Li baterije i Li||LiFePO4 baterije sastavljene su u pretincu za rukavice. Maseni omjer LiFePO4, Ketjen crnog i poliviniliden difluorida (PVDF) u materijalu katode je 90 : 5 : 5, a površinski kapacitet je 0,67 mAh·cm-2. Pogledajte Dodatni materijal S1 za pojedinosti o procesu pripreme ploče pozitivne elektrode i postupku sastavljanja baterije.
1.3 Metode karakterizacije materijala
Funkcionalne skupine i kemijske strukture PEGDA monomera i njihovih polimera analizirane su pomoću Thermo NiColet iS50 Fourier Transform Infracrvenog spektrometra (Fourier Transform Infrared Spectrometer, FT-IR) tvrtke Thermo Fisher Scientific Corporation iz Sjedinjenih Država, s rasponom valne duljine od {{ 2}} cm-1. Kristalnost elektrolita u gel-stanju s različitim sadržajem polimera karakterizirana je D2 Phaser rendgenskim difraktometrom (X-Ray Diffractometer, XRD) tvrtke Bruker AXS, Njemačka, a raspon skeniranja bio je 2θ=5 stupnjeva ~ 80 stupnjeva. Instrument za mjerenje kontaktnog kuta OCA40Micro tvrtke Beijing Dongfang Defei Instrument Co., Ltd. korišten je za testiranje kontaktnog kuta otopina prekursora s različitim sadržajem PEGDA na površini LiFePO4 ploče elektrode. Mikroskopska morfologija poprečnog presjeka i površine litijevog metalnog lima promatrana je JElectronics JSM-7500F skenirajućim elektronskim mikroskopom s emisijom polja (Emisioni skenirajući elektronski mikroskop, FESEM). Elementarne informacije na površini litijevog metalnog lima analizirane su korištenjem fotoelektronskog spektrometra X-zraka Escalab 250Xi (X-ray Photoelectron Spectroscopy, XPS) tvrtke Thermo Fisher Scientific Corporation iz Sjedinjenih Država.
1.4 Elektrokemijsko ispitivanje
Prozor elektrokemijske stabilnosti elektrolita ispitan je linearnom sweep voltametrijom (LSV), raspon napona bio je od napona otvorenog kruga (OCV) do 6 V, a brzina sweep-a bila je 1 mV·s-1. Frekvencijski raspon spektroskopije elektrokemijske impedancije (EIS) je 10-2~106 Hz, a napon poremećaja je 10 mV. Kronoamperometrijom je mjeren migracijski broj litijevih iona u elektrolitu, razlika potencijala postavljena je na 10 mV, a vrijeme 800 s, te je migracijski broj litijevih iona dobiven prema formuli (1):

Među njima, tLi plus je broj prijenosa litijevih iona, ΔV je razlika potencijala, R{{0}} i RS su vrijednosti impedancije sučelja elektrode i elektrolita prije i poslije ispitivanja, redom, i I0 i IS su struja početnog stanja, odnosno struja stacionarnog stanja. Sva gornja ispitivanja provedena su na višekanalnoj elektrokemijskoj radnoj stanici PARSTAT MC tvrtke AMETEK, SAD. Performanse ciklusa punjenja i pražnjenja baterije testirane su pomoću platforme za testiranje baterija LAND CT3001A-1U tvrtke Wuhan Landian Electronics Co., Ltd.
2 Rezultati i rasprava
2.1 Priprema i strukturna analiza GCE
U ovoj studiji PEGDA je korišten kao monomer, AIBN je korišten kao inicijator polimerizacije, a EC i DEC su uvedeni kao plastifikatori. Elektrolit u gel stanju s umreženim polimernim polietilen glikol dimetakrilatom (p(PEGDA)) sintetiziran je na 70 stupnjeva. Formula reakcije polimerizacije prikazana je na slici 1(a). Nakon dodavanja toplinskog inicijatora AIBN, PEGDA s dvije aktivne terminalne C=C skupine brzo se podvrgava intermolekularnoj homopolimerizaciji kada se zagrije na 70 stupnjeva. Aktivni lanci AIBN-a povezuju molekularne lance jedan s drugim ili iznutra, i konačno dobivaju p(PEGDA) mrežnu kosturnu strukturu, te uspješno koriste metodu polimerizacije na licu mjesta za dobivanje elektrolita u stanju gela unutar baterije. Kao što je prikazano na slici S1, sve tri otopine prekursora s različitim sadržajem PEGDA pokazale su dobru sposobnost vlaženja na limu pozitivne elektrode LiFePO4, što je ključ za postizanje dobrog međupovršinskog kontakta između elektrolita i elektrode.
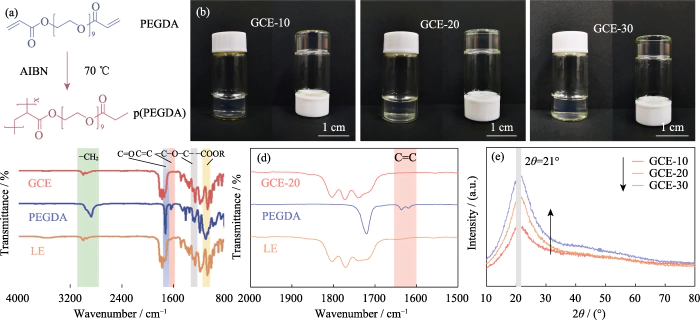
Slika 1. Priprema i strukturna analiza GCE
(a) Reakcija polimerizacije PEGDA; (b) optičke fotografije GCE-x; (c, d) FT-IR spektri GCE-20, PEGDA i LE; (e) XRD uzorci GCE-x; Šarene figure dostupne su na web stranici
Kako bi se dobio GCE s visokom ionskom vodljivošću, LiTFSI, koji ima visok stupanj disocijacije u polimeru, korišten je kao litijeva sol, a 0.2 mol/L LiDFOB uveden je za konstrukciju mreže gela sustav dvostruke soli. LiDFOB ima dobru topljivost i toplinsku stabilnost, posebno u svojstvima stvaranja filma. Kada su karbonatna otapala u kontaktu s metalnim litijevim anodama, vjerojatno će se na površini metalnog litija formirati veliki broj labavih poroznih ili dendritičnih slojeva taloženja litija. Uvođenje LiDFOB-a može pomoći u stvaranju međufaznog sloja čvrstog elektrolita bez HF (Solid Electrolyte Interphase, SEI) i poboljšati kompatibilnost s litijevim metalnim anodama. U isto vrijeme, LiTFSI ima korozivni učinak na metalne kolektore struje, dok LiDFOB može pasivizirati metalni aluminij i ublažiti korozijski učinak LiTFSI na kolektore struje. Međutim, elektrolit s jednom soli LiDFOB-a pokazao je veću impedanciju od LiTFSI-LiDFOB elektrolita s dvije soli iste koncentracije. Kao što je prikazano na slici S2, Li||LiFePO4 baterija sastavljena je pomoću 1,2 mol/L LiDFOB odnosno LiTFSI-LiDFOB gel elektrolita, a impedancija LiTFSI-LiDFOB baterije bila je znatno manja.
Postojeći rezultati istraživanja pokazuju da LiTFSI i LiDFOB mogu imati sinergistički učinak, učinkovito poboljšavajući kompatibilnost elektrolita s litijevom metalnom anodom. Jiao Shuhong i sur. upotrijebio XPS i FT-IR kako bi otkrio da elektrolit dvostruke soli LiTFSI i LiDFOB može pasivizirati aluminijski kolektor struje pozitivne elektrode i formirati stabilan SEI sloj na površini litijeve metalne negativne elektrode kako bi se postiglo dugoročno stabilno cikliranje litij metalnih baterija. Na temelju toga, Liu Yue et al. [26] koristili su hibridnu simulaciju molekularne dinamike za proučavanje zajedničkog mehanizma djelovanja LiTFSI i LiDFOB u litijevim metalnim baterijama i objasnili zaštitni učinak LiTFSI na LiDFOB. Studije su pokazale da je BO veza LiDFOB-a relativno najslabija i sklona pucanju. LiDFOB će se brzo razgraditi pod djelovanjem slobodnih radikala i reagirati s metalnim litijem stvarajući slobodne atome Li0 i bora. Reakcija umetanja atoma bora uzrokuje razgradnju molekula otapala u elektrolitu, a rezultirajući molekularni fragmenti nastavit će reagirati s molekularnim fragmentima litijeve soli i atomima bora. U sustavu dilitijeve soli, međutim, LiTFSI se prvenstveno razgrađuje, oslanjajući se na "mehanizam žrtvovanja" za zaštitu LiDFOB-a, stopa razgradnje LiDFOB-a značajno je smanjena. Time se smanjuje broj slobodnih atoma Li0 i bora, što može optimizirati SEI sloj i zaštititi litijevu metalnu anodu.
Kao što je prikazano na slici 1(b), GCE-x je ujednačen i proziran kao žele, nije više tekući. Za daljnju provjeru polimerizacije monomera, FT-IR je korišten za karakterizaciju kemijskih struktura LE, PEGDA monomera i GCE-20. Kao što je prikazano na slici 1(c), sva tri uzorka pokazuju tipični vrh apsorpcije C=O vibracije rastezanja (~1726 cm-1). Vrh apsorpcije na 1280 cm-1 GCE odgovara vrhovima antisimetričnog i simetričnog rastezanja eterske veze, što ukazuje da -(CH2CH2)n- u monomeru nije uništen tijekom polimerizacije. Vrhovi na 1095 i 2867 cm−1 pripadaju -COOR odnosno -CH2. Kao što je prikazano na slici 1(d), karakteristični vrh C=C veze PEGDA nalazi se na 1616-1636 cm-1, ali nestaje u GCE, što ukazuje da je PEGDA bila potpuno polimerizirao.
Budući da litijevi ioni migriraju samo u amorfnom području GCE-a, smanjenje kristalnosti elektrolita je korisno za poboljšanje ionske vodljivosti. Slika 1(e) je XRD uzorak GCE-x. Sva tri tipa uzoraka imaju jedinstveni vrh apsorpcije difrakcije na 2θ=21 stupnja, što ukazuje da pripremljeni elektrolit ima amorfno područje praćeno malom količinom kristalita. Kako se sadržaj PEGDA povećava, područje vrha spektra se značajno povećava, udio amorfnog područja gel elektrolita se smanjuje, a sadržaj amorfnih komponenti u elektrolitu se smanjuje, što ne pogoduje migraciji iona.
2.2 Elektrokemijska izvedba analize kompatibilnosti GCE i Li metala
Kako bi se proučila kompatibilnost elektrolita s različitim sadržajem polimera s litijevim metalnim anodama u baterijama, analizirani su spektri impedancije Li||Li simetričnih baterija s GCE-x elektrolitima u početnom stanju (kao što je prikazano na slici S3). Na slici su vrijednosti impedancije sučelja GCE-10 i GCE-20 baterije male, 93 odnosno 152 Ω, a GCE-30 baterija doseže 409 Ω. To pokazuje da migracija litijevih iona u GCE-u s višim sadržajem polimera mora prevladati veću migracijsku barijeru, koja ne pogoduje brzom provođenju litijevih iona na međupovršini.
Promatrajući prenapon Li||Li simetrične baterije u testu ciklusa punjenja i pražnjenja, možemo znati razliku potencijala generiranu migracijom ionskog para tijekom ovog procesa, a zatim procijeniti ponašanje taloženja/skidanja litija. Slika S4 prikazuje krivulje napon-vrijeme Li||Li simetrične ćelije GCE-x. Ispitna temperatura bila je 25 stupnjeva, a baterija se punila i praznila pod konstantnom strujom sa specifičnim kapacitetom od 0.5 mAh cm-2 i gustoćom struje od 0.5 mA cm-2. Početni prenapon Li|GCE-10|Li stanica bio je 22 mV, a napon je porastao na 137 mV nakon 250 h. Prenapon simetrične baterije GCE-30 bio je 104 mV u početnoj fazi, a prenapon je brzo rastao u narednim ciklusima, dosegnuvši vršnu vrijednost od 509 mV u 227 h, a zatim je naglo pao, što ukazuje da je baterija imala unutarnji kratki spoj. Suprotno tome, baterija GCE-20 može raditi na niskom prenaponu blizu 30 mV i ima najstabilnije elektrokemijske performanse. Sljedeće će se usredotočiti na GCE-20 elektrolit.
Ionska vodljivost elektrolita izravno odražava sposobnost iona da migriraju u električnom polju. Ionska vodljivost LE i GCE{{0}} ispitana je na 60, 50, 40, 30, 20, 10 i 0 stupnjeva, redom. Kao što je prikazano na slici 2(a), ionska vodljivost GCE-20 na 30 stupnjeva je 1.00 mS cm-1, a kada temperatura ispitivanja poraste na 60 stupnjeva, vodljivost doseže 1,39 mS cm-1. To je zato što aktivacijska energija opada s porastom ispitne temperature, a aktivnost kretanja segmenata polimernog lanca i litijevih iona raste. Međutim, na brzinu kretanja segmenata polimernog lanca očito utječe temperatura, tako da se vodljivost GCE-20 gel elektrolita mijenja više nego vodljivost otopine elektrolita.

Slika 2. Elektrokemijska izvedba GCE-20
(a) Ionske vodljivosti LE i GCE-20; (b) LSV krivulje LE i GCE-20; (c) Trenutno-vremenski profil Li|GCE-20|Li ćelije s umetkom koji prikazuje odgovarajuće Nyquistove dijagrame; (d) Krivulje napon-vrijeme simetričnih Li||Li ćelija sastavljenih s LE i GCE-20; (e) Nyquistov dijagram Li|GCE-20|Li ćelije nakon cikliranja; (f) Krivulje napon-vrijeme i gustoća struje-vrijeme Li|GCE-20|Li ćelije; Šarene figure dostupne su na web stranici
Poboljšanje gustoće energije baterija zahtijeva osiguranje stabilnosti elektrolita pri visokim radnim naponima. Studije su pokazale da karbonil-koordinirani elektroliti na bazi polimera obično imaju širok elektrokemijski prozor i dobru stabilnost pri visokim radnim naponima. Slika 2(b) pokazuje da LSV krivulja GCE-20 baterije počinje značajno fluktuirati na 5,26 V, te se može smatrati da elektrokemijski prozor GCE-20 gel elektrolita doseže 5,26 V. Nasuprot tome, elektrokemijski prozor komercijalnog elektrolita je samo 3,92 V. Stoga, elektrolit u gel stanju ima izvrsnu elektrokemijsku stabilnost pri visokom naponu.
Osim toga, migracijski broj litij-iona elektrolita također je jedan od pokazatelja za mjerenje vodljivosti litij-iona. Definira se kao omjer broja litijevih iona koji prolaze kroz dio elektrolita okomito na smjer migracije litijevih iona po jedinici vremena prema zbroju aniona i kationa koji prolaze kroz dio. Što je viša vrijednost, to je veći udio litijevih iona u procesu migracije iona i veća je učinkovitost migracije. Slika 2(c) je kronoamperometrijska krivulja Li|GCE-20|Li baterije, gdje je umetak usporedba elektrokemijske impedancije baterije prije i poslije testa. Prema formuli (1), migracijski broj litij-iona GCE-20 je 0.21. Uvođenjem aditiva ili dopinga s anorganskim punilima može se postići veća stopa migracije litij iona, što nije samo korisno za poboljšanje brzine punjenja i pražnjenja baterije, već također povećava stabilnost ciklusa.
Tijekom procesa punjenja i pražnjenja Li||Li simetrične baterije, anioni i kationi u elektrolitu prolaze kroz protumigraciju. Prilikom punjenja ioni litija migriraju na negativnu elektrodu, a anioni migriraju na pozitivnu elektrodu, a kod pražnjenja je obrnuto. Stoga, tijekom procesa punjenja i pražnjenja, gradijent koncentracije iona između pozitivne i negativne elektrode i ugrađeno električno polje postupno se povećavaju, ometajući suprotno kretanje aniona i kationa, što rezultira polarizacijom koncentracije unutar baterije, što rezultira promjenom u prenaponu. Kao što je prikazano na slici 2(d), Li|GCE-20|Li baterija ima prenapon od 46 mV nakon stabilnog ciklusa od 300 h. Međutim, prenapon koji generira Li|LE|Li baterija tijekom testa znatno je veći nego kod Li|GCE-20|Li baterije (65~118 mV). To je zato što rastući dendriti litija uzrokuju lagane kratke spojeve na nekim unutarnjim mjestima. Rezultati pokazuju da je elektrokemijsko ponašanje unutar GCE-20 baterije idealnije. Slika 2(e) je EIS test simetrične baterije nakon 10, 20, 50 i 100 ciklusa. Kako se broj ciklusa punjenja i pražnjenja povećava, impedancija baterije ima tendenciju smanjenja. Tijekom ovog procesa izgrađen je stabilan SEI sloj između elektrolita i metalnog sučelja litija, a kontakt sučelja je optimiziran, tako da se impedancija sučelja značajno smanjila.
Na 25 stupnjeva, Li|GCE-20|Li baterija bila je podvrgnuta 10 ciklusa punjenja i pražnjenja pri gustoći struje od 0.2, {{10} }.5, 1, 2, 0,2 i 0,5 mA cm-2, redom. Slika 2(f) odražava trend prenapona simetrične ćelije tijekom vremena tijekom ovog procesa. Prenapon pri niskoj gustoći struje je malen i može ostati relativno stabilan. Nakon što se gustoća struje poveća, prenapon se u skladu s tim povećava i nema naglog povećanja/smanjenja napona tijekom procesa.
Morfologija sloja litijevog sloja nakon ciklusa može vizualno karakterizirati taloženje/skidanje litija unutar baterije. Li||Li simetrična baterija rastavljena je nakon punjenja i pražnjenja od 100 h pri kapacitetu od 0,5 mAh cm-2 i gustoći struje od 0,5 mA cm{{6} }, a mikroskopska morfologija poprečnog presjeka i površine litijevog metalnog lima promatrana je FESEM-om. Kao što je prikazano na slici 3(a, b), debljina neobrađene ploče čistog litija je 353 µm, a površina je ravna i glatka. Interakcija između tekućeg elektrolita i metalnog litija dovodi do taloženja velikog broja rastresitih i poroznih slojeva taloženja litija na površini litijeve ploče Li|LE|Li baterije, uglavnom u obliku fine i neravne mahovine. Kada se debljina litijevog metalnog lima poveća na 446 µm, dolazi do očitog učinka ekspanzije volumena i stvara se veliki broj dendrita. Nasuprot tome, debljina litijskog sloja u Li|GCE-20|Li bateriji je 391 μm, a sloj površinskog taloženja je gust i ujednačen, te nema fino usitnjene litijeve prevlake (Sl. 3(c). )). To pokazuje da elektrolit u gel stanju može učinkovito potisnuti ekspanziju volumena litijeve metalne anode. LiDFOB u GCE-20 može pomoći u formiranju stabilnog SEI sloja za uravnoteženje unutarnjeg potencijala baterije i odgoditi rast litijevih dendrita induciranjem ravnomjernog taloženja litija. Stoga, u određenoj mjeri, može optimizirati taloženje/skidanje litija i zaštititi litijevu metalnu anodu.

Slika 3 SEM slike metalnog Li
Poprečni presjek (gore) i pogled odozgo (dolje) SEM slike (a) morfologije taloženja svježeg metalnog Li i litija u simetričnim Li||Li ćelijama s (b) LE i (c) GCE-20
Naknadno je korištena XPS analiza površinskih elemenata za istraživanje sastava SEI sloja na površini litijeve metalne anode pod djelovanjem LiTFSI-LiDFOB sustava dvostrukih soli GCE. Slika S5 je XPS spektar površine litijeve metalne anode korištenjem LE i GCE-20. Spektar C1s (Sl. S5(a, d)) uglavnom ima 4 vrha signala, koji odgovaraju CC/CH na 284,8 eV. Dva vrha na 286,4 i 289,4 eV odgovaraju CO odnosno C=O, a uglavnom su izvedeni iz produkata razgradnje karbonatnih otapala (kao što su ROCO2-, ROC-, itd.) . Vrh na 292,7 eV odgovara CF3, koji uglavnom potječe iz proizvoda razgradnje litijevih soli. U O1s spektru (Slika S5(b, e)), vrhovi na 531,1 i 532,3 eV odgovaraju C=O odnosno CO, a relativni sadržaj CO značajno je smanjen, što je uglavnom povezano s smanjenje udjela produkata razgradnje. Pod zajedničkim djelovanjem LiTFSI i LiDFOB, ograničeno je stvaranje LiOCH3, Li2O2C2H4 i drugih nusproizvoda. Osim toga, za razliku od LE (Sl. S5(e)), u F1s spektru GCE-20 (Sl. S5(f)), vrh signala LiF je na 684,5 eV, a LiF može pomoći u stvaranje gustog i stabilnog SEI sloja.
2.3 Analiza elektrokemijskih svojstava Li||LiFePO4 baterije
LiFePO4 ima prednosti velikog kapaciteta, dugog životnog ciklusa i izvanredne sigurnosti te je glavni aktivni materijal pozitivne elektrode. Njegov teorijski specifični kapacitet je 170 mAh·g-1. Na 25 stupnjeva, Li|GCE-20|LiFePO4 baterija je punjena i ispražnjena 200 puta pri konstantnoj struji od 0,2C (1C=0,67 mA·cm{{12 }}). Kao što je prikazano na slici 4(a,b), specifični kapacitet pražnjenja prvog ciklusa je 141,4 mAh·g-1. Specifični kapacitet pražnjenja 200. kruga je 131,4 mAh·g-1, stopa zadržavanja kapaciteta doseže 92,95 posto, a smanjenje kapaciteta s jednim okretajem je manje od 0,04 posto. Napon platforme je stabilan, u skladu sa karakteristikama LiFePO4 baterija. Kulonska učinkovitost, kao važan pokazatelj za ocjenu stabilnosti ciklusa baterije, odnosi se na omjer kapaciteta pražnjenja baterije i kapaciteta punjenja tijekom istog ciklusa. Kulonska učinkovitost prvog ciklusa Li|GCE-20|LiFePO4 baterije je 97,8 posto. Zbog formiranja SEI sloja tijekom procesa pražnjenja prvog ciklusa, generira se dio ireverzibilnog kapaciteta, što rezultira niskom kulonskom učinkovitošću prvog ciklusa.

Slika 4. Elektrokemijska izvedba Li|GCE-20|LiFePO4 ćelija
(a) Performanse ciklusa i (b) odgovarajuće krivulje napon-kapacitet na 0.2C; (c) performanse brzine i (d) odgovarajuće krivulje napon-kapacitet; Šarene figure dostupne su na web stranici
Osim toga, provedena su ispitivanja punjenja i pražnjenja na Li|GCE{{0}}|LiFePO4 na 0.3C, 0.5C, 1C, 1.5C i {{12 }}.5C brzine struje kako biste istražili njenu brzinu. Kao što je prikazano na slici 4(c), kada je brzina struje 0.5C, specifični kapacitet pražnjenja prvog ciklusa baterije je 160.2 mAh·g-1. Kako se brzina struje povećava, specifični kapacitet pražnjenja baterije opada unutar kontroliranog raspona. Brzina se povećava na 2C, a specifični kapacitet prvog ciklusa pražnjenja je 130 mAh·g-1. Nakon toga, strujna brzina ponovno se vratila na 0,5 C, a specifični kapacitet prvog ciklusa pražnjenja bio je 156,1 mAh·g-1. Relevantne krivulje napon-kapacitet prikazane su na slici 4(d). Napon platoa pri različitim brzinama je stabilan bez uzroka povećanja prenapona, a baterija pokazuje dobre performanse brzine i reverzibilnost.
3 Zaključak
GCE na bazi PEGDA razvijen je toplinskim iniciranjem polimerizacije na licu mjesta. FT-IR i XRD analiza karakterizacije GCE-a, u kombinaciji s elektrokemijskim testovima, pokazala je optimalnu GCE formulaciju. Nadalje sastavite bateriju kako biste proučili elektrokemijsku izvedbu elektrolita i analizirali zaštitni učinak elektrolita na negativnu elektrodu metalnog litija promatrajući mikroskopsku morfologiju i karakterizaciju elementa površine metalnog litija, objašnjavajući:
1) GCE-x (x=10, 20, 30) pripremljen polimerizacijom na licu mjesta može dobro namočiti ploču elektrode, a elektrolit ima najbolju elektrokemijsku stabilnost kada je maseni udio PEGDA 20 posto.
2) Uveden je sustav dilitijeve soli LiTFSI i LiDFOB, koji može stvoriti dobru interakciju s komponentama polimera. Elektrolit ima širok elektrokemijski prozor (5,26 V) i visoku ionsku vodljivost (30 stupnjeva, 1×10-3 S·cm-1). U isto vrijeme, sustav dilitijeve soli može se koristiti za izradu stabilnog SEI sloja i učinkovitu zaštitu litijeve metalne anode.
3) Upotrebom GCE-20 za usklađivanje s komercijalnim katodnim materijalom LiFePO4, sastavljena puna baterija može se stabilno puniti i prazniti 200 ciklusa pri struji od 0,2C, sa stopom zadržavanja kapaciteta od 92,95 posto , i pokazuje dobre performanse brzine.
Ukratko, ovim radom dobivena je sigurna i izvrsna elektrokemijska izvedba GCE-a, koja pruža učinkovito rješenje za razvoj sigurnih i stabilnih litij-metalnih baterija visoke gustoće energije.
Dodatni materijal:
Proces pripreme baterije S1
Pomiješajte i sameljite LiFePO4, Ketjen crni i PVDF u skladu s ciljanim omjerom, dodajte otapalo N-metilpirolidon (N-metilpirolidon, NMP), dobro promiješajte i dispergirajte te dobijete jednoličnu i viskoznu kašu aktivnog materijala. Suspenzija je struganjem obložena na aluminijskoj foliji s ravnim premazom, zatim prebačena u vakuumsku pećnicu i sušena na 80 stupnjeva 12 h. Nakon rezanja ploče elektrode, ponovno je osušite i premjestite u bezvodnu pretinac za rukavice bez kisika.
Brtva, šrapnel i metalni list od litija postavljeni su redom u središte kućišta negativne elektrode, a debljina metalnog lista od litija bila je 0,35 mm. Nakon toga, otopina prekursora GCE dodana je kap po kap na središte površine negativne elektrode (50 µL) pomoću pištolja za pipetu, a zatim su Celgard 2500 separator baterija i sloj pozitivne elektrode (Celgard 2500 separator baterija) stavljeni u slijed. Prije sastavljanja Li||LiFePO4 baterije izvagan je pozitivni pol i zabilježeno je opterećenje aktivnim materijalom. Površinsko opterećenje aktivnog materijala LiFePO4 pozitivne elektrode bilo je 3,94 mg cm-2. Na kraju, stavite bateriju pod tlak i zatvorite je na stroju za brtvljenje baterija, premjestite je u okolinu od 70 stupnjeva i zagrijavajte 2 sata kako biste započeli polimerizaciju kako biste dobili elektrolit u stanju gela. Kako bi se osiguralo da elektrolit potpuno uđe u LiFePO4 polni dio, bateriju je potrebno ostaviti da odstoji 1 sat nakon sastavljanja.

Slika S1 Kontaktni kutovi između otopine polimernog prekursora i katoda
(a) LE; (b) GCE-10; (c) GCE-20; (d) GCE-30

Slika S2 Nyquistovi dijagrami GCE sastavljenih Li||LiFePO4 ćelija s različitim litijevim solima

Slika S3 Nyquistovi dijagrami simetričnih Li||Li ćelija sastavljenih s GCE-x elektrolitima

Slika S4 Naponsko-vremenski profili simetričnih Li||Li ćelija sastavljenih s GCE-x elektrolitima

Slika S5 XPS spektri metalne Li anode u simetričnim Li||Li ćelijama
(a, d) C1s, (b, e) O1s, (c, f) F1s XPS spektri metalne Li anode s (ac) LE i (df) GCE-20
[1] GOODENOUGH JB, KIM Y.
Izazovi za punjive Li baterije
Kemija materijala, 2010, 22(3):587.
[2] ZHAO J, LIAO L, SHI F, et al.
Površinsko fluoriranje anodnih materijala reaktivnih baterija za povećanu stabilnost
Časopis Američkog kemijskog društva, 2017., 139(33):11550.
[3] TARASCON JM, ARMAND M.
Problemi i izazovi s kojima se suočavaju punjive litijeve baterije
Nature, 2001, 414(6861):359.
[4] ZHI J, YAZDI AZ, VALAPPIL G, et al.
Međufaza umjetnog krutog elektrolita za vodene litijeve sustave za pohranu energije
Znanstveni napredak, 2017., 3(9):e1701010.
[5] JUN K, SUN Y, XIAO Y, et al.
Litijevi superionski vodiči s okvirima koji dijele kutove
Nature Materials, 2022, 21: 924.
[6] LIU J, BAO Z, CUI Y, et al.
Putovi za praktične visokoenergetske dugotrajne litij metalne baterije
Energija prirode, 2019, 4(3):180.
[7] DUNN B, KAMATH H, TARASCON J M.
Skladištenje električne energije za mrežu: baterija izbora
Znanost, 2011, 334(6058):928.
[8] MAUGER A, JULIEN CM, PAOLELLA A, et al.
Izrada boljih baterija u čvrstom stanju: pregled
Materijali, 2019, 12(23):3892.
[9] MANTHIRAM A, YU X, WANG S.
Kemikalije litijskih baterija omogućene elektrolitima u čvrstom stanju
Nature Reviews Materials, 2017, 2(4):16103.
[10] ZHOU D, SHANMUKARAJ D, TKACHEVA A, et al.
Polimerni elektroliti za baterije na bazi litija: napredak i izgledi
Chem, 2019, 5(9):2326.
[11] TAN SJ, YUE J, TIAN YF, et al.
In-situ inkapsulacija vatrootpornog fosfata u robusnu polimernu matricu za sigurne i stabilne kvazi-solid-state litij metalne baterije
Materijali za pohranu energije, 2021, 39: 186.
[12] ZHAO Q, LIU X, STALIN S, et al.
Polimerni elektroliti u čvrstom stanju s ugrađenim brzim međufaznim transportom za sekundarne litijeve baterije
Energija prirode, 2019, 4(5):365.
[13] ZHOU Z, FENG Y, WANG J, et al.
Robusna, vrlo rastezljiva ionsko provodljiva obloga za stabilne litij metalne baterije
Chemical Engineering Journal, 2020, 396: 125254.
[14] WILKEN S, TRESKOW M, SCHEERS J, et al.
Početne faze toplinske razgradnje elektrolita litij-ionske baterije na bazi LiPF6-detaljne Ramanove i NMR spektroskopije
RSC Advances, 2013, 3(37):16359.
[15] LIU FQ, WANG WP, YIN YX, et al.
Nadogradnja tradicionalnog tekućeg elektrolita putem in situ gelacije za buduće litij metalne baterije
Znanstveni napredak, 2018., 4(10):eaat5383.
[16] XU C, SUN B, GUSTAFSSON T, et al.
Formiranje međusloja u litijevim baterijama s čvrstim polimernim elektrolitom: XPS studija
Journal of Materials Chemistry A, 2014, 2(20):7256.
[17] WEI Z, CHEN S, WANG J, et al.
Vrhunska vodljivost litij-iona polimernog elektrolita sa češljastom strukturom putem kopolimerizacije bez otapala za bipolarnu litij bateriju u čvrstom stanju
Journal of Materials Chemistry A, 2018, 6(27):13438.
[18] DI NOTO V, LAVINA S, GIFFIN GA i sur.
Polimerni elektroliti: sadašnjost, prošlost i budućnost
Electrochimica Acta, 2011, 57(15):4.
[19] XUE Z, HE D, XIE X.
Elektroliti na bazi poli(etilen oksida) za litij-ionske baterije
Journal of Materials Chemistry A, 2015, 3(38):19218.
[20] MINDEMARK J, LACEY MJ, BOWDEN T, et al.
Osim PEO-alternativnih materijala domaćina za Li plus -provodljive čvrste polimerne elektrolite
Progress in Polymer Science, 2018, 81: 114.
[21] ARAVINDAN V, GNANARAJ J, MADHAVI S, et al.
Litij-ionske vodljive soli elektrolita za litijeve baterije
Chemistry-A European Journal, 2011, 17(51):14326.
[22] XU K.
Elektroliti i međufaze u Li-ion baterijama i šire
Chemical Reviews, 2014, 114(23):11503.
[23] YANG H, ZHUANG GV, ROSS JR P N.
Toplinska stabilnost soli LiPF6 i elektrolita Li-ionske baterije koji sadrže LiPF6
Journal of Power Sources, 2006, 161(1):573.
[24] LI Q, LIU G, CHENG H, et al.
Dizajn niskotemperaturnog elektrolita za litij-ionske baterije: izgledi i izazovi
Chemistry-A European Journal, 2021, 27(64):15842.
[25] JIAO S, REN X, CAO R, et al.
Stabilno cikliranje visokonaponskih litij metalnih baterija u eterskim elektrolitima
Energija prirode, 2018, 3(9):739.
[26] LIU Y, YU P, SUN Q, et al.
Predviđena operando polimerizacija na litij anodi putem umetanja bora
ACS Energy Letters, 2021, 6(6):2320.
[27] CAO W, LU J, ZHOU K, et al.
Organsko-anorganski kompozit SEI za stabilnu Li metalnu anodu polimerizacijom na licu mjesta
Nano energija, 2022, 95: 106983.
[28] CHENG S, SMITH DM, LI C Y.
Kako kristalna struktura nanomjera utječe na transport iona u čvrstim polimernim elektrolitima?
Macromolecules, 2014, 47(12):3978.
[29] JOHANSSON P.
Prvi principi modeliranja amorfnih polimernih elektrolita: kompleksi Li plus -PEO, Li plus -PEI i Li plus -PES
Polymer, 2001, 42(9):4367.
[30] SUN B, MINDEMARK J, EDSTRÖM K, et al.
Čvrsti polimerni elektroliti na bazi polikarbonata za Li-ion baterije
Solid State Ionics, 2014, 262: 738.
[31] SILVA MM, BARROS SC, SMITH MJ, et al.
Karakterizacija čvrstih polimernih elektrolita na bazi poli (trimetilenkarbonata) i litijeva tetrafluoroborata
Electrochimica Acta, 2004, 49(12): 1887.
[32] BARBOSA P, RODRIGUES L, SILVA MM, et al.
Karakterizacija čvrstih polimernih elektrolita pTMCnLiPF6
Solid State Ionics, 2011, 193(1):39.





